 2020.03.20
2020.03.20  1651次
1651次
新冠肺炎疫情目前已经全球爆发,不仅医护人员每日奋战在一线,科研人员也一直在背后进行机制、药物、疫苗的研究。从2019年12月爆发开始,仅仅三个多月,就已经发表论文600多篇。这些论文,为我们认识、预防、治疗新冠病毒,提供了极大的帮助。对于没有临床样本的科研人员,怎么利用现有的数据来进行相关研究呢?接下来,我们来看看从结构、RNA seq和单细胞RNA seq三个不同角度分析的案例。

图片来自清华大学AMiner团
1、案例一
从基因组开始,再到结构、到蛋白表达,逐步解开COVID-19的谜团!

题目:2019-nCoV(COVID-19)与受体结合的结构分析
01、研究背景
SARS-CoV中尖峰糖蛋白在病毒表面形成尖峰,尖峰蛋白的受体结合域(RBD)与宿主ACE2受体结合,从而进入宿主细胞。2019-nCoV(COVID-19)与SARS-CoV高度相似,对2019-nCoV(COVID-19) 的RBD与受体结合的结构分析,对于病毒的防治尤其重要。
02、方法与结果
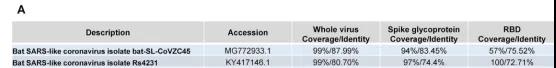
从GenBank 数据库中下载到2019-nCoV(COVID-19)序列,并将序列用BLAST方法与NCBI数据库中的序列进行比对,结果发现最接近2019-nCoV(COVID-19)的同源物是从蝙蝠(MG772933.1)中分离出的SARS冠状病毒,序列同源性为87.99%,覆盖率为99%。其次是从人或者麝猫中分离出的SARS冠状病毒。在2019-nCoV(COVID-19)的整个基因组中,编码尖峰糖蛋白的区域(最不保守的区域)与SARS-CoV序列同源性为74-83%。2019-nCoV(COVID-19)序列中的RBD与SARS-CoV也有72%-76%的同源性(图A)。以上结果显示,与SARS-CoV相同,2019-nCoV(COVID-19)的受体可能也是ACE2。
将2019-nCoV(COVID-19)的RBD 3D结构与SARS-CoV的进行叠合,发现两个结构基本重合,仅有loop2处有一点差异(图ABC)。
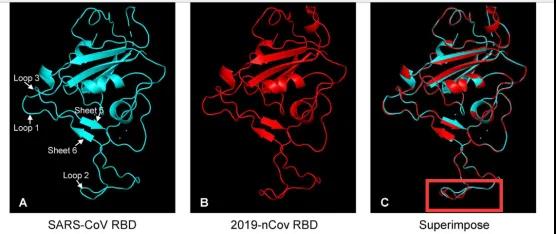
为了研究RBD与ACE2的结合,作者进行了分子对接,发现2019-nCoV(COVID-19)和SARS-CoV具有类似的与ACE2结合模式,但是2019-nCoV(COVID-19)结合能力更强。在SARS-CoV 的RBD中有16个氨基酸残基与ACE2直接接触,其中8个在2019-nCoV(COVID-19)中保守,推测2019-nCoV(COVID-19)中特有的氨基酸可能增强了与ACE2的互作。
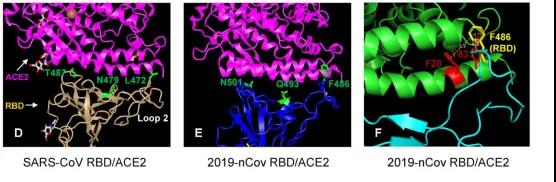
为了确定变异氨基酸对RBD与ACE2相互作用的贡献,作者比较了其他三种SARS-CoV相关病毒的RBD序列,通过结构分析,解释了2019-nCoV(COVID-19)感染能力更强的原因。

另外作者还探究了ACE2在动物界的分布,发现ACE2在鱼类、两栖动物、爬行动物、鸟类、哺乳动物均有表达,并且它们的同源性很高,表明这些动物均有可能是2019-nCoV(COVID-19)的宿主。
通过进行免疫染色,作者发现ACE2在肺泡上皮细胞以及动脉和静脉内皮细胞、动脉平滑肌细胞、肾小管上皮和小肠上皮中均有表达,为2019-nCoV(COVID-19)和SARS-CoV通过肺的气道感染提供了强有力的证据。
通过检索人类蛋白质图谱数据库,作者发现小ACE2在肠,结肠,十二指肠,肾脏,睾丸和胆囊均有表达,并且表达水平高于肺。ACE2的组织表达模式提示了其他可能涉及肠道、肾脏、睾丸和其他组织功能的病毒传播模式。
03、结论
高度同源的序列、尖峰糖蛋白编码序列和RBD序列,推测2019-nCoV(COVID-19)与SARS-CoV类似,具有相同的受体ACE2。结构重叠、分子对接和结构分析,解释了2019-nCoV感染力更强的原因。ACE2在其他动物的表达水平分析,表明这些动物都可能是宿主。ACE2在人体不同器官中的表达水平分析,提示除呼吸系统传播外,其他传播途径也要引起重视。
2、案例二
TCGA 癌旁RNA seq数据也有巨大的挖掘价值!

题目:2019-nCoV(COVID-19) ACE2受体在口腔粘膜上皮细胞中高表达
01、研究背景
据报道,ACE2是2019-nCoV(COVID-19)的宿主细胞主要受体,在病毒进入细胞引起最终感染中起着至关重要的作用,因此表达ACE2的细胞可能作为靶细胞,具有很大的研究价值。
02、方法和结果
从癌症基因组图谱(TCGA)数据库中搜集到13种器官的癌旁正常组织的RNA-seq数据。从哺乳动物基因组cap分析的功能注释(FANTOM5 CAGE)数据库中搜集到14种正常组织器官的RNA-seq数据。作者探究了不同组织的ACE2表达情况,结果发现两个数据库均显示在口腔粘膜可以表达ACE2。
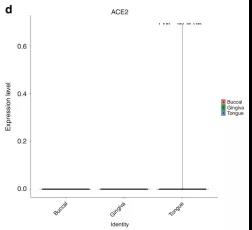
为了研究ACE2在口腔粘膜上的表达,根据TCGA提供的部位信息,作者探究了ACE2在不同口腔部位的表达情况。研究发现:当将舌底、口底和口腔其他部位与舌进行比较时,发现舌中ACE2的平均表达明显高于其他部位(图c)。将舌与其他口腔中其他部位相比较时,舌中ACE2的表达也是处于较高水平(图d)。
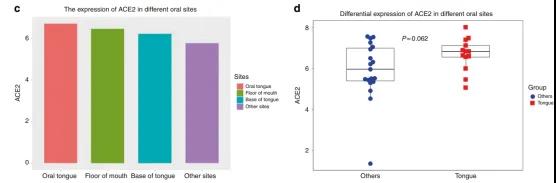
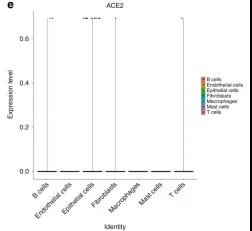
接下来对口腔组织(舌、颊和舌)进行单细胞测序,并对数据进行分析,结果发现口腔组织中有0.52% ACE2阳性细胞,这些细胞95.86%来源于舌(图d)。单细胞测序将细胞分为7类,其中95.86%的ACE2阳性细胞来源于上皮细胞图(e)。上述结果表明,ACE2可在口腔粘膜上皮细胞上表达,并在舌上皮细胞中高度富集。
03、结论
这些发现解释了口腔是2019-nCoV(COVID-19)易感性潜在高风险的基本机制,并为牙科临床实践和日常生活中的预防策略提供了一份证据。
3、案例3
除了口腔,其他身体部位的潜在风险也要探究!

题目:对ACE2受体表达的单细胞RNA-seq数据分析揭示了不同人体器官易受2019-nCoV(COVID-19)感染的潜在风险
01、研究背景
在2019-nCoV(COVID-19)感染期间,具有ACE2表达的肺AT2细胞可能是主要的靶细胞。然而,一些患者也表现出非呼吸症状,如肾衰竭,这意味着2019-nCoV(COVID-19)也可能侵染其他器官。研究人体不同器官的风险,具有重要意义。
02、方法和结果
作者从GEO数据库中搜集了来自主要人类生理系统,包括呼吸系统、心血管系统、消化系统和泌尿系统的单细胞RNA测序(Scrna-seq)数据集。
作者对来自鼻黏膜、气管、支气管和肺的单细胞测序数据进行分析,结果发现 ACE2阳性AT2细胞的平均比例约为1%。一个被普遍接受的共识表明,2019-nCoV(COVID-19)病毒倾向于通过宿主受体ACE2攻击肺AT2细胞,因此将ACE2在AT2细胞中的表达水平作为参考,平均比例高于1%的ACE2阳性细胞被认为是高风险的,低于此标准的细胞被认为是低风险的。
随后作者对不同器官的ACE2阳性细胞水平进行了分析并对细胞类型进行了鉴定,确定了处于高风险的器官,如肺、心脏、食道、肾脏、膀胱和回肠,同时也确定了特定的细胞类型(即II型肺泡细胞(AT2)、心肌细胞、肾近端小管细胞、回肠和食道上皮细胞以及膀胱尿路上皮细胞),这些细胞易受2019-nCoV(COVID-19)感染。
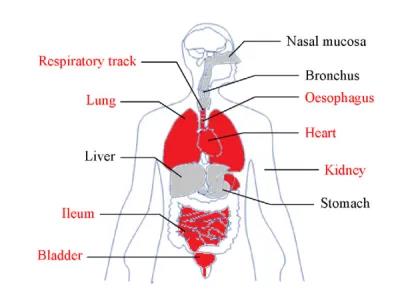
03、结论
构建人体不同器官的风险图,可为进一步研究2019-nCoV(COVID-19)感染的发病机制和途径提供潜在线索。
即使没有临床样本,合理运用现有的数据,也可以帮助我们对COVID-19进行研究,为疫情的防控贡献出一份力量。



 返回列表
返回列表